製品・サービス情報
|
|
HaemoScan社製品
血液関連アッセイキット・バイオマーカー検出キット |
|
 |
HaemoScan社では、血液と生体材料の相互作用を評価できるキットや自然免疫活動(補体活性)を評価できるテストキット、バイオマーカー検出キットをラインナップしています。
 AP50テスト(代謝経路補体活性) AP50テスト(代謝経路補体活性)
|
代替経路法(AP50 )は、Mg++の存在下でのウサギ赤血球の溶解に基づいています。補体の枯渇や欠乏が疑われる場合のスクリーニング検査として役立ちます。このテストは、経路の成分の現象、欠如および不活性に敏感です。
この方法は、補体成分の阻害または消費に対する医薬品の影響を評価する場合にも適しています。
◆アプリケーション
◆原理
|
赤血球懸濁液を段階希釈した血清または血漿とともに、37℃で30分間インキュベートします。
補体系の活性化は溶血を引き起こします。インキュベーション後、サンプルを遠心分離して上清を取得します。補体活性に正比例する上清中の遊離ヘモグロビン濃度は、415nmの波長で分光光度計を使用して測定されます。溶血の程度に対して血漿の希釈係数をプロットすると、AP50の計算が可能になります。(つまり、赤血球の50%の溶解を得るための血漿の希釈)このキットは、少量サンプル(75μL)で代替経路を介して補体活性を測定する様に設計されており、96well(丸底)マイクロプレートで実行可能です。アッセイは、マイクロ遠心チューブで行うことができます。 |
|
 |
◆保管と安定性
◆参考文献
|
1. |
Pinnapireddy
SR , Giselbrecht J , Strehlow B , Janich C , Husteden C , Meister A , Loppnow H
, Sedding D , Erdmann F , Hause G , Brezesinski G , Groth T , Langner A ,
Bakowsky U , Wölk C . A triple chain polycationic peptide-mimicking amphiphile
- efficient DNA-transfer without co-lipids. Biomater Sci. 2019 Dec
17;8(1):232-249. |
|
2. |
Giselbrecht J, Wiedemann S,
Reddy Pinnapireddy S, Goergen N, Loppnow H, Sedding D, Erdmann F, Bakowsky U,
Hause G, Lúcio M, Langner A, Wölk C. Nucleic acid carrier composed of a
branched fatty acid lysine conjugate-Interaction studies with blood components.
Colloids Surf B Biointerfaces. 2019 Dec 1;184:110547.
|
◆価格
|
| 製品名 |
サイズ |
税別価格 |
カタログ# |
マニュアル |
MSDS |
| AP50 Assay |
100回 |
お問合せ |
K001 |
 |
 |
|
|
 CH50テスト(古典的経路補体活性) CH50テスト(古典的経路補体活性)
|
古典経路法(CH50)は、Ca++およびMg++の存在下で感作されたヒツジ赤血球の溶解に基づいています。
補体の枯渇や欠乏が疑われる場合のスクリーニング検査として役立ちます。このテストは、経路の成分の減少、欠如および不活性に敏感です。この方法は、補体成分の阻害または消費に対する医薬品の影響を評価する場合にも適しています。
◆アプリケーション
◆原理
|
赤血球懸濁液を段階希釈した血清または血漿とともに37℃で30分間インキュベートします。
補体系の活性は溶血を引き起こします。インキュベーション後、サンプルを遠心分離して上清を取得します。補体活性に正比例する上清中の遊離ヘモグロビン濃度は、415nmの波長で分光光度計を使用して測定されます。溶血の程度に対して血漿の希釈係数をプロットすると、CH50の計算が可能になります。(つまり、赤血球の50%の溶解を得るための血清の希釈)
このキットは、少量のサンプル(25μL)の古典的経路を介して補体活性を測定する様に設計されており、96ウェル(丸底)マイクロプレートで実行可能です。アッセイは、マイクロ遠心チューブでも行うことができます。 |
|
 |
◆保存と安定性
◆参考文献
|
1. |
Pinnapireddy
SR , Giselbrecht J , Strehlow B , Janich C , Husteden C , Meister A , Loppnow H
, Sedding D , Erdmann F , Hause G , Brezesinski G , Groth T , Langner A ,
Bakowsky U , Wölk C . A triple chain polycationic peptide-mimicking amphiphile
- efficient DNA-transfer without co-lipids. Biomater Sci. 2019 Dec
17;8(1):232-249. |
|
2. |
Giselbrecht
J, Wiedemann S, Reddy Pinnapireddy S, Goergen N, Loppnow H, Sedding D, Erdmann
F, Bakowsky U, Hause G, Lúcio M, Langner A, Wölk C. Nucleic acid carrier
composed of a branched fatty acid lysine conjugate-Interaction studies with
blood components. Colloids Surf B Biointerfaces. 2019 Dec 1;184:110547. |
|
3. |
Garaulet G, Lazcano
JJ, Alarcón H, de Frutos S, Martínez-Torrecuadrada JL, Rodríguez A. Display of
the Albumin-Binding Domain in the Envelope Improves Lentiviral Vector
Bioavailability. Hum Gene Ther Methods. 2017 Dec;28(6):340-351. |
|
4. |
Akhouri
RR, Goel S, Furusho H, Skoglund U, Wahlgren M. Architecture of Human IgM in
Complex with P. falciparum Erythrocyte Membrane Protein 1. Cell Rep. 2016 Feb
2;14(4):723-736. |
|
5. |
Misra
SK, Chang HH, Mukherjee P, Tiwari S, Ohoka A, Pan D. Regulating
Biocompatibility of Carbon Spheres via Defined Nanoscale Chemistry and a
Careful Selection of Surface Functionalities. Sci Rep. 2015 Oct 14;5:14986. |
|
6. |
Mukherjee
P, Misra SK, Gryka MC, Chang HH, Tiwari S, Wilson WL, Scott JW, Bhargava R, Pan
D. Tunable Luminescent Carbon Nanospheres with Well-Defined Nanoscale Chemistry
for Synchronized Imaging and Therapy. Small. 2015 Sep;11(36):4691-703. |
|
7. |
Luo J, Lindstrom J. Antigen-specific immunotherapeutic vaccine for experimental
autoimmune myasthenia gravis. J Immunol. 2014 Nov 15;193(10):5044-55. |
◆価格
|
| 製品名 |
サイズ |
税別価格 |
カタログ# |
マニュアル |
MSDS |
| CH50 Assay |
100回 |
お問合せ |
K002 |
 |
 |
|
|
 補体コンバターゼアッセイ 補体コンバターゼアッセイ
|
補体コンバターゼ測定は、生体材料による補体活性化を決定するための高感度で特異的な方法です。
血漿とのインキュベーション中に、補体因子が材料の表面に結合し、続いて補体コンバターゼ複合体が形成されます。洗浄後、結合していない補体タンパク質を除去するために、生体材料を特定の発色基質を含む培地でインキュベートします。基質の裂開は、405nmの光学密度を測定することによって定量化されます。
◆アプリケーション
◆原理
|
対象の試験物質(理想的には表面積を知る必要があります)を血漿としてインキュベートします。インキュベート中、補体因子が材料の表面に結合し、続いて補体コンパターゼ複合体が形成されます。
インキュベーション後、サンプルを洗浄し、補体コンパターゼ特異的発色基質を用いて補体コンパターゼ活性を分析します。発色率は生体材料の表面で生成されたコンパターゼの量に依存します。 |
|
 |
◆保管と安定性
◆参考文献
|
1. |
Fernández-Colino
A, Wolf F, Rütten S, Schmitz-Rode T, Rodríguez-Cabello JC, Jockenhoevel S, Mela
P. Small Caliber Compliant Vascular Grafts Based on Elastin-Like Recombinamers for
in situ Tissue Engineering. Front Bioeng Biotechnol. 2019 Nov 19;7:340. |
|
2. |
Wiegand C,
Abel M, Hipler UC, Elsner P, Zieger M, Kurz J, Wendel HP, Stoppelkamp S.
Hemostatic wound dressings: Predicting their effects by in vitro tests. J
Biomater Appl. 2019 Apr;33(9):1285-1297.
|
| |
3. |
Naso F,
Stefanelli U, Buratto E, Lazzari G, Perota A, Galli C, Gandaglia A. Alpha-Gal
Inactivated Heart Valve Bioprostheses Exhibit an Anti-Calcification Propensity
Similar to Knockout Tissues. Tissue Eng Part A. 2017 Oct;23(19-20):1181-1195.
|
| |
4. |
Aguiari P,
Iop L, Favaretto F, Fidalgo CM, Naso F, Milan G, Vindigni V, Spina M, Bassetto
F, Bagno A, Vettor R, Gerosa G. In vitro comparative assessment of
decellularized bovine pericardial patches and commercial bioprosthetic heart
valves. Biomed Mater. 2017 Feb 3;12(1):015021.
|
| |
5. |
Diaz-Gomez
L, Alvarez-Lorenzo C, Concheiro A, Silva M, Dominguez F, Sheikh FA, Cantu T,
Desai R, Garcia VL, Macossay J. Biodegradable electrospun nanofibers coated
with platelet-rich plasma for cell adhesion and proliferation. Mater Sci Eng C
Mater Biol Appl. 2014 Jul 1;40:180-8.
|
| |
6. |
Gladitz
M, Bauer J, Brückner P, Reinemann S, Wiegand C, Zieger M, Reddersen K, Hipler
U, Frant M, Liefeith K, Radusch H. Antibacterial polyamides based on a
dendritic zinc-hybrid with good biocompatibility showing reduced biofilm
formation, BioNanoMaterials, 2014, 15(1-2), 31-46.
|
|
7. |
Jovanovic D, et al. Polyacylurethanes as novel degradable cell carrier
materials for tissue engineering. Materials, 2011, 4.10: 1705-1727.
|
|
8. |
Jovanovic D,
Engels GE, Plantinga JA, Bruinsma M, van Oeveren W, Schouten AJ, van Luyn MJ,
Harmsen MC. Novel polyurethanes with interconnected porous structure induce in
vivo tissue remodeling and accompanied vascularization. J Biomed Mater Res A.
2010 Oct;95(1):198-208.
|
◆価格
|
| 製品名 |
サイズ |
税別価格 |
カタログ# |
マニュアル |
MSDS |
| Complement Convertase Assay |
30回 |
お問合せ |
K005 |
 |
 |
|
|
 溶血アッセイ 溶血アッセイ
|
溶血活性は、血液に接触する医療機器についてテストする必要があります。
この試験は、接触、浸出物、毒素、金属イオン、表面電荷、その他赤血球溶解の原因によって引き起こされる赤血球溶解に基づいています。生体材料と赤血球懸濁液の直接接触に基づいており、ヘモグロビンの放出を分光光度計で測定します。
◆アプリケーション
◆原理
|
赤血球懸濁液は、37℃で回転させながら試験物質とともに24時間インキュベートします。インキュベーションの前後にサンプルを採取、遠心分離を行い、遊離ヘモグロビンを含む上清を取得します。ヘモグロビン濃度は分光光度計により測定されます。テストサンプルは、標準物質と比較されます。キットには陽性反応と反応性の低い標準物質が含まれています。各分析には少なくとも2つの標準物質を含めることを推奨します。標準物質に関連して試験された材料の結果は、溶血活性を評価するために使用することも可能です。良否の基準は2%の溶血に基づいていることに注意する必要があります。したがって、使用した赤血球懸濁液の総ヘモグロビン濃度も決定する必要があります。このキットは少量の生体材料サンプルの溶血活性を測定する様に設計されています。 |
|
 |
◆保管と安定性
◆参考文献
|
1. |
Franco
AR, Fernandes EM, Rodrigues MT, Rodrigues FJ, Gomes ME, Leonor IB, Kaplan DL,
Reis RL. Antimicrobial coating of spider silk to prevent bacterial attachment
on silk surgical sutures. Acta Biomater. 2019 Nov;99:236-246. |
|
2. |
Wersig
T, Krombholz R, Janich C, Meister A, Kressler J, Mäder K. Indomethacin
functionalised poly(glycerol adipate) nanospheres as promising candidates for
modified drug release. Eur J Pharm Sci. 2018 Oct 15;123:350-361.
|
| |
3. |
Shi J, So LY,
Chen F, Liang J, Chow HY, Wong KY, Wan S, Jiang T, Yu R. Influences of
disulfide connectivity on structure and antimicrobial activity of tachyplesin
I. J Pept Sci. 2018 Jun;24(6):e3087.
|
| |
4. |
Nemani
KV, Moodie KL, Brennick JB, Su A, Gimi B. In vitro and in vivo evaluation of
SU-8 biocompatibility. Mater Sci Eng C Mater Biol Appl. 2013 Oct;33(7):4453-9.
|
◆価格
|
| 製品名 |
サイズ |
税別価格 |
カタログ# |
マニュアル |
MSDS |
| Hemolysis Assay |
30回 |
お問合せ |
K003 |
 |
 |
|
|
 N-アセチル-グルコサミニダーゼアッセイ N-アセチル-グルコサミニダーゼアッセイ
|
N-アセチル-グルコサミニダーゼ(NAG)は、腎臓の尿細管系が損傷した後、尿中に排泄されます。
この損傷は、腎虚血後に発生するか、炎症反応によって引き起こされる可能性があります。尿素を同時測定後、尿細管損傷の定量的測定値を取得して、希釈を補正することが可能です。NAGは基質変換アッセイで決定されます。
適切な条件下で、尿中のNAGは発色基質を変換し、色の発生後、光学密度で測定されます。
濃度(U/L)は、既知の濃度の酵素を使用したスタンダードを適用することで定量化されます。
◆アプリケーション
◆原理
|
酵素N-アセチル-グルコサミニダーゼ(NAG)は、腎臓近位尿細管損傷のマーカーとして使用可能です。
サンプルは発色基質とともにインキュベートします。低pHで1時間インキュベートした後、塩基性停止液を添加し、400nmの光学密度を測定します。サンプルには高いバックグラウンドシグナルをもたらす可能性のある成分が含まれている可能性があるため、全てのサンプルのブランク値は反応後ではなく、反応前に停止液が追加され測定されます。NAGの濃度は、U/Lで表され、ユニットの酵素は、pH4.25、25℃で1分あたり、1mmolの基質を変換可能です。 |
|
 |
◆保管と安定性
◆参考文献
|
1. |
Gerritsen KG, Leeuwis
JW, Koeners MP, Bakker SJ, van Oeveren W, Aten J, Tarnow L, Rossing P, Wetzels
JF, Joles JA, Kok RJ, Goldschmeding R, Nguyen TQ. Elevated Urinary Connective
Tissue Growth Factor in Diabetic Nephropathy Is Caused by Local Production and
Tubular Dysfunction. J Diabetes Res. 2015;2015:539787. |
|
2. |
Vermeulen
Windsant IC, de Wit NC, Sertorio JT, van Bijnen AA, Ganushchak YM, Heijmans JH,
Tanus-Santos JE, Jacobs MJ, Maessen JG, Buurman WA. Hemolysis during cardiac
surgery is associated with increased intravascular nitric oxide consumption and
perioperative kidney and intestinal tissue damage. Front Physiol. 2014 Sep
8;5:340.
|
| |
3. |
de
Haan JJ, Windsant IV, Lubbers T, Hanssen SJ, Hadfoune M, Prinzen FW, Greve JW,
Buurman WA. Prevention of hemolysis-induced organ damage by nutritional
activation of the vagal anti-inflammatory reflex*. Crit Care Med. 2013
Nov;41(11):e361-7.
|
| |
4. |
van
Wijck K, Lenaerts K, van Loon LJ, Peters WH, Buurman WA, Dejong CH.
Exercise-induced splanchnic hypoperfusion results in gut dysfunction in healthy
men. PLoS One. 2011;6(7):e22366.
|
| |
5. |
Nauta FL, Boertien
WE, Bakker SJ, van Goor H, van Oeveren W, de Jong PE, Bilo H, Gansevoort RT.
Glomerular and tubular damage markers are elevated in patients with diabetes.
Diabetes Care. 2011 Apr;34(4):975-81.
|
| |
6. |
Snoeijs
MG, van Bijnen A, Swennen E, Haenen GR, Roberts LJ 2nd, Christiaans MH,
Peppelenbosch AG, Buurman WA, Ernest van Heurn LW. Tubular epithelial injury
and inflammation after ischemia and reperfusion in human kidney
transplantation. Ann Surg. 2011 Mar;253(3):598-604.
|
|
7. |
Meijer E, Boertien WE, Nauta FL, Bakker SJ, van Oeveren W, Rook M, van
der Jagt EJ, van Goor H, Peters DJ, Navis G, de Jong PE, Gansevoort RT.
Association of urinary biomarkers with disease severity in patients with
autosomal dominant polycystic kidney disease: a cross-sectional analysis.
Am J Kidney Dis. 2010 Nov;56(5):883-95.
|
|
8. |
Vermeulen
Windsant IC, Snoeijs MG, Hanssen SJ, Altintas S, Heijmans JH, Koeppel TA,
Schurink GW, Buurman WA, Jacobs MJ. Hemolysis is associated with acute kidney
injury during major aortic surgery. Kidney Int. 2010 May;77(10):913-20.
|
|
9. |
Morariu
AM, Schuurs TA, Leuvenink HG, van Oeveren W, Rakhorst G, Ploeg RJ. Early events
in kidney donation: progression of endothelial activation, oxidative stress and
tubular injury after brain death. Am J Transplant. 2008 May;8(5):933-41.
|
|
10. |
Huybregts
RA, Morariu AM, Rakhorst G, Spiegelenberg SR, Romijn HW, de Vroege R, van Oeveren
W. Attenuated renal and intestinal injury after use of a mini-cardiopulmonary
bypass system. Ann Thorac Surg. 2007 May;83(5):1760-6.
|
◆価格
|
| 製品名 |
サイズ |
税別価格 |
カタログ# |
マニュアル |
MSDS |
| N-Acetyl-glucosaminidase Assay |
96回 |
お問合せ |
K006 |
 |
 |
|
|
 トロンビン生成アッセイ トロンビン生成アッセイ
|
トロンビンは凝固カスケードの重要な酵素です。その測定は生体材料の血栓形成能力(すなわち、血餅を形成する能力)に関する直接的な情報を提供します。通常血漿では、トロンビンはフィブリン網目構造に捕捉され、アンチトロンビンIIIまたは他のアンチプロテアーゼによって急速に不活性化されます。トロンビンの半減期が短いため、正確な酵素測定が妨げられます。
HaemoScan社が設計したこのキットは、生体材料にさらされた後のインキュベーション培地でのトロンビン活性の測定を可能にする特殊な血漿に基づいています。
◆アプリケーション
◆原理
|
TAGは生体材料の血栓形成性を示します。生体材料を改変血漿中でインキュベートした時のトロンビン形成の量および測定を測定し、標準物質と比較します。キットには反応性の高いものと反応性の低い標準物質(1種類の金属と2種類のポリマー)が含まれています。各分析には少なくとも2つの標準物質を含めることを推奨します。テストサンプルの活性と比較するために、標準物質を選択することも可能です。材料をはじめ血漿中でインキュベートされます。
TGA試薬を添加後、トロンビンの生成が始まります。様々な時点でトロンビンの生成が測定されます。トロンビンの濃度は、トロンビン特異的な発色基質との酵素反応によって決定され、トロンビンの量に比例した黄色の生成物が得られます。サンプルのトロンビン濃度は、検量線から決定可能です。各材料のトロンビン生成曲線は、サンプルが採取された時点に対するトロンビン濃度をプロットすることによって作成されます。この曲線は、cm2サンプルあたりで表されるトロンビン生成の速度を決定するために使用されます。標準物質に関連する試験された材料の結果は、血栓形成性を評価するためにも使用可能です。
このキットは少量の生体材料のトロンビン生成活性を測定する様に設計されています。 |
|
 |
◆保管と安定性
◆参考文献
|
1. |
Echeverry-Rendon M, Duque V, Quintero D, Robledo
SM, Harmsen MC, Echeverria F. Improved corrosion resistance of commercially
pure magnesium after its modification by plasma electrolytic oxidation with
organic additives. J Biomater Appl. 2018 Nov;33(5):725-740 |
|
2. |
Naso F,
Stefanelli U, Buratto E, Lazzari G, Perota A, Galli C, Gandaglia A. Alpha-Gal
Inactivated Heart Valve Bioprostheses Exhibit an Anti-Calcification Propensity
Similar to Knockout Tissues. Tissue Eng Part A. 2017 Oct;23(19-20):1181-1195. |
| |
3. |
Jovanovic
D, et al. Polyacylurethanes as novel degradable cell carrier materials for
tissue engineering. Materials, 2011, 4.10: 1705-1727.
|
| |
4. |
Jovanovic D,
Engels GE, Plantinga JA, Bruinsma M, van Oeveren W, Schouten AJ, van Luyn MJ,
Harmsen MC. Novel polyurethanes with interconnected porous structure induce in
vivo tissue remodeling and accompanied vascularization. J Biomed Mater Res A.
2010 Oct;95(1):198-208.
|
| |
5. |
Krenning
G, van der Strate BW, Schipper M, van Seijen XJ, Fernandes BC, van Luyn MJ,
Harmsen MC. CD34+ cells augment endothelial cell differentiation of CD14+
endothelial progenitor cells in vitro. J Cell Mol Med. 2009 Aug;13(8B):2521-33.
|
| |
6. |
Krenning
G, Dankers PY, Drouven JW, Waanders F, Franssen CF, van Luyn MJ, Harmsen MC,
Popa ER. Endothelial progenitor cell dysfunction in patients with progressive
chronic kidney disease. Am J Physiol Renal Physiol. 2009 Jun;296(6):F1314-22.
|
◆価格
|
| 製品名 |
サイズ |
税別価格 |
カタログ# |
マニュアル |
MSDS |
| Thrombin Generation Assay |
20回 |
お問合せ |
K004 |
 |
 |
|
|
 化学発光ELISA基質 化学発光ELISA基質
|
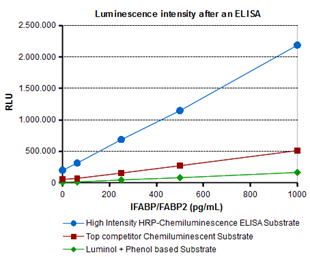
HaemoScan 高強度HRP-化学発光ELISA基質は、強化された化学発光式を使用しており、競合他社の製品の最大4倍の強度、標準のルミノール+フェノールベース基質の最大13倍の強度の発光シグナルをもたらします。(図1)
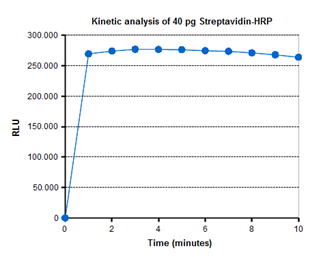
この基質の発光シグナルは数分以内に最大に達します(図2)。発光ベースのELISAは通常黒または白の不透明なマイクロプレートで実行されますが、チューブで実行される場合もあります。
 |
|
図1. ルミノールベースのHaemoScan高強度HRP-化学発光ELISA基質を使用した高強度光シグナル
腸の脂肪酸結合タンパク質(IFABP/FABP2)キャリブレータ―は、白色の不透明なNunc Maxisorpマイクロプレートを使用した酵素結合免疫吸着測定法(ELISA)によって室温で分析されました。最後のインキュベーションステップ(ストレプトアビジン-HRP)の後、マイクロプレートをバッファーで洗浄し、ウェルあたり100μLの基質を添加しました。プレートシェーカー上で10秒間インキュベートした後、1分間に発光を測定しました。 |
 |
|
図2. ルミノールベースのHaemoScan高強度HRP化学発光ELISA基質による迅速な光生成
ストレプトアビジンーHRPを希釈し、白色の不透明なNuncMaxisorpマイクロプレートに50μL移しました。50μLのHaemoScan高強度HRP化学発光ELISA基質を添加した後、マイクロプレートをシェーカー上で室温で10秒間インキュベートし、1分間隔で発光を測定しました。 |
◆特長
|
・高いシグナル強度(標準的なルミノール+フェノールベース基質の最大13倍のシグナル)
・迅速な光生成(最大シグナルは数分以内に生成)
・広いダイナミックレンジ(ピコグラムレベルまでの検出)
・高いS/N比(低いバックグラウンド)
・取り扱いが簡便(2つの内容物を1:1に混合するだけ)
・便利な保管(室温で出荷および保管可能) |
◆アプリケーション
|
西洋ワサビペルオキシダーゼ(HRP)活性を検出するための強化された化学発光基質であり、ELISAでピコグラムレベルのタンパク質を検出する様に最適化されています。 |
◆原理
|
西洋ワサビペルオキシダーゼなどのペルオキシダーゼは、過ホウ酸塩などの触媒の存在下で、ルミノールの3-アミノフタレートへの酸化を触媒します。この反応には、425nmの発光が伴います。
化学発光ベースのELISAは、ルミノメーターを使用して相対光単位(RLU)を測定することによって定量化されます。酵素・基質反応が起こった後も持続する着色生成物を生成する比色(発色)基質とは対照的に、化学発光基質は酵素・基質反応中にのみ光を生成し、すぐに測定することが可能です。 |
◆保管と安定性
◆参考文献
◆価格
|
| 製品名 |
サイズ |
税別価格 |
カタログ# |
マニュアル |
MSDS |
| High Intensity Chemiluminescence ELISA Substrate |
100mL |
お問合せ |
R001-100ml |
 |
 |
| 250mL |
お問合せ |
R001-250ml |
| 500mL |
お問合せ |
R001-500ml |
| 2x500mL |
お問合せ |
R001-2x500ml |
|
|
|
|
【お問合せ】
|
試薬機器部
Phone 052-624-4388
  |
|
|
|
|
| Copyright (C) Filgen, Inc. All Rights Reserved. |
|